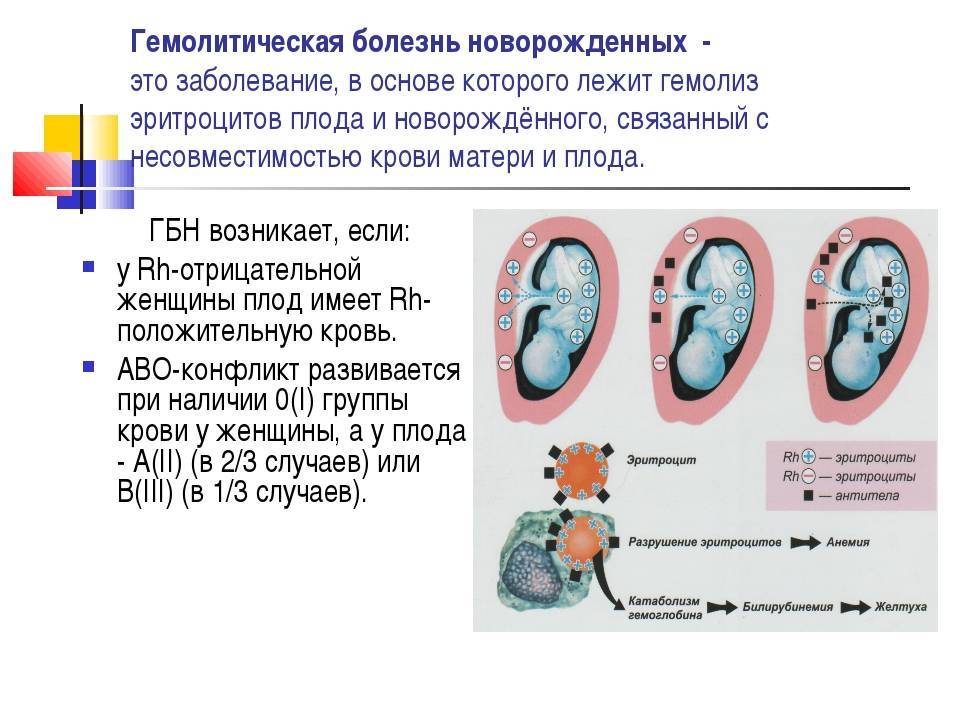
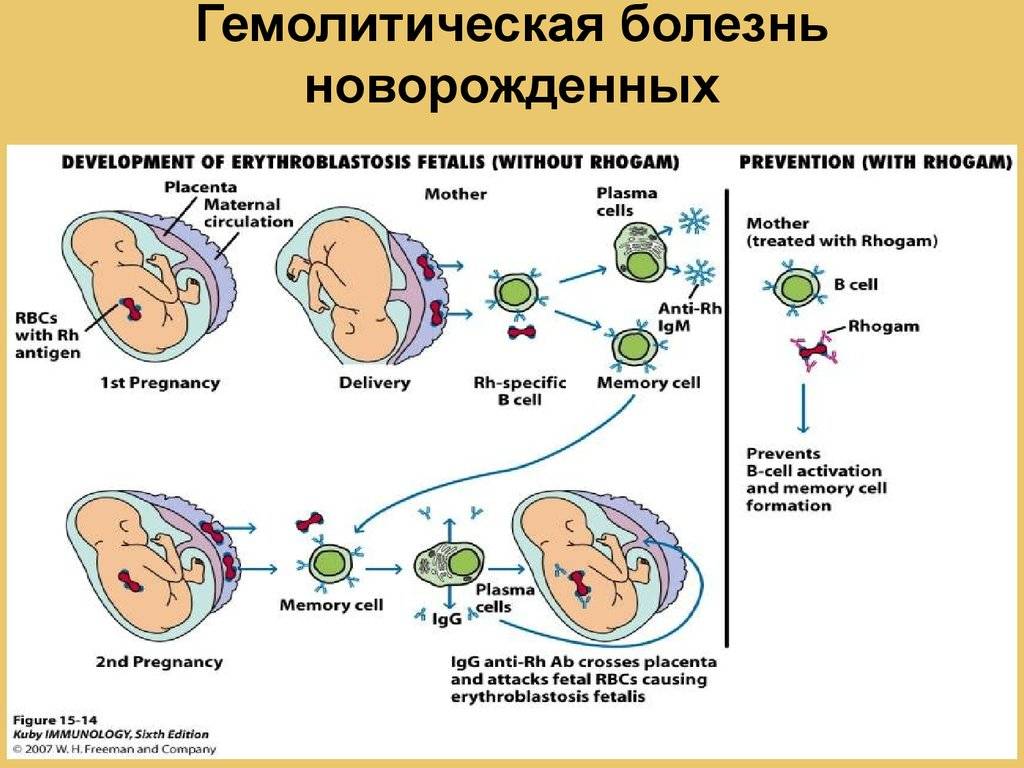
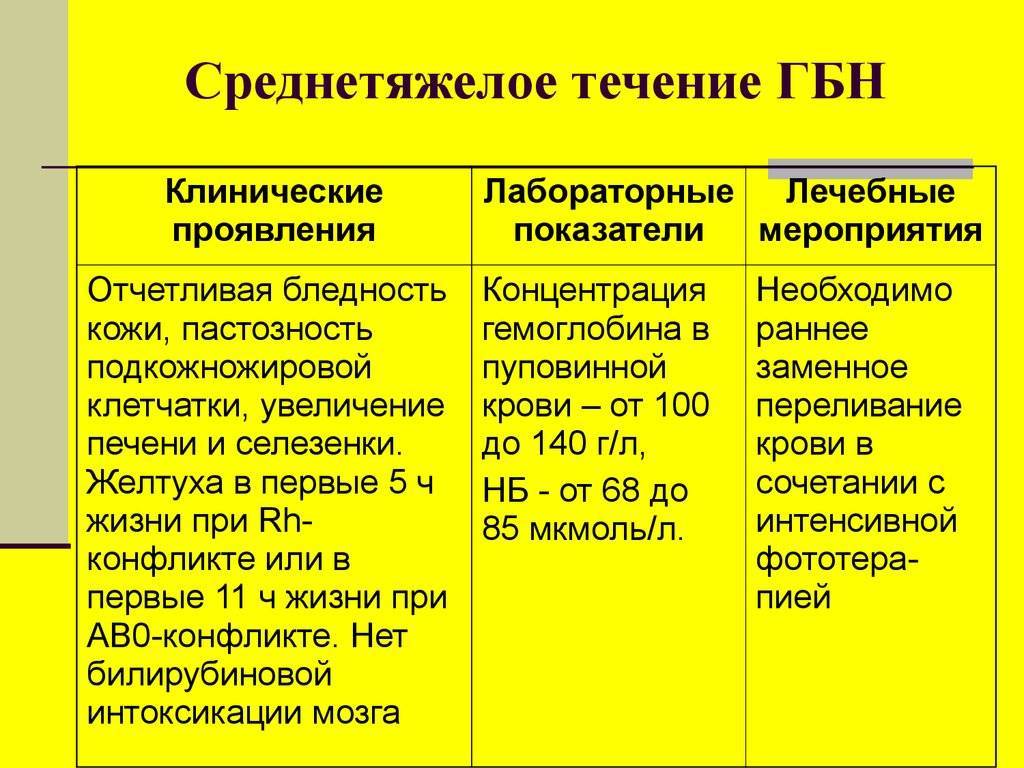
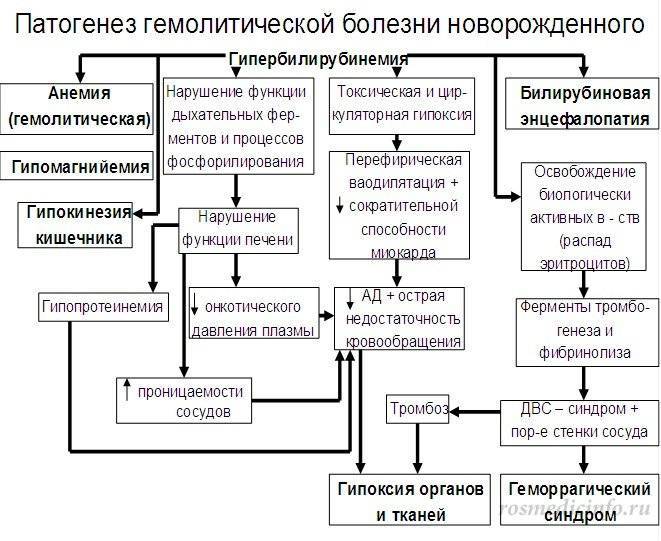
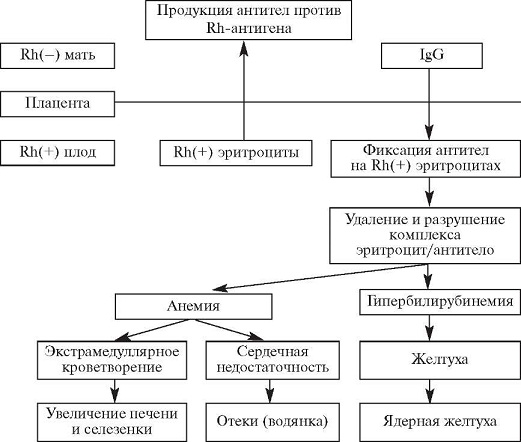
2 возможные причины гемолитической болезни новорождённых
Содержание статьи
- Патологическая анатомия
- Патофизиология
- Специфические антитела
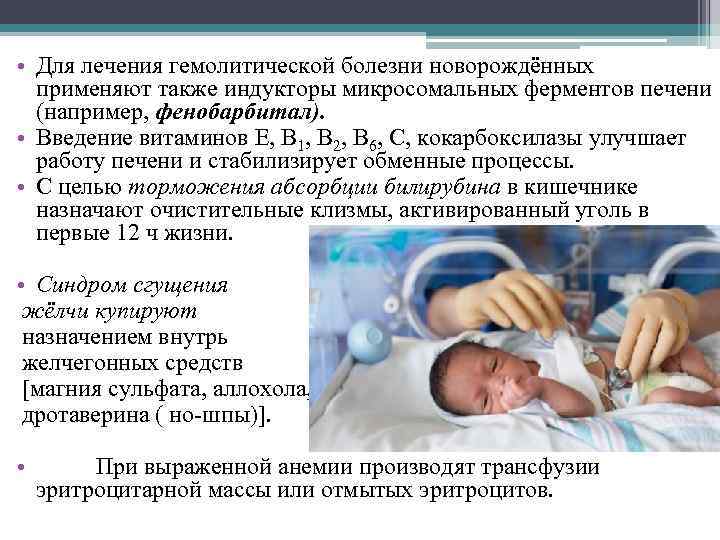
- Лечение ГБН
- Диагноз
- В каких формах развивается ГНБ
- Самая распространенная форма ГБН
- Симптомы
- Чем опасна желтуха новорожденных
- Самая редкая форма ГБН
- Симптомы
- Самая легкая форма ГБН
- Симптомы
- Прогноз по группе крови и резус-фактору
- Резус-фактор и возникновение конфликта по этому признаку
- Конфликт по признаку группы крови и его проявления
- Таблица: потенциально опасные сочетания групп крови матери и плода
- Таблица: потенциально опасные сочетания групп крови матери и отца
- Лечение
- Неинвазивные методы
- Инвазивные методы
- Фототерапия
- Применение иммуноглобулина
- Инфузионная терапия
- Оперативная терапия
- Выбор препаратов для заменного переливания крови
- Симптомы и признаки
- Желтушная
- Анемическая
- Отёчная
- Причины и картина развития гемолитической болезни новорожденного и плода
Патологическая анатомия
Патологоанатомические изменения при внутриутробной смерти плода при сроке беременности V—VII мес. (ранняя фетопатия) скудные. Изучение их затрудняется из-за аутолиза и мацерации.
Рис. 21. Эритробластоз печени. Обилие эритробластов и нормобластов (темные клетки) в синусоидах печени при отечной форме гемолитической болезни новорожденных (окраска гематоксилин-эозином; х 400).
Рис. 22. Накопление гемосидерина (синего цвета) в макрофагах красной пульпы селезенки при желтушной форме гемолитической болезни новорожденных (окраска по Перльсу; х 400).
Рис. 23. Острое набухание, ишемические изменения нейронов (указано стрелками) в аммоновом роге головного мозга при желтушной форме гемолитической болезни новорожденных (окраска по Нисслю; х 400).
Отечная форма Г. б. н. характеризуется общими значительными отеками, кожа плода бледная, полупрозрачная, блестящая, частично мацерированная, с петехиальными кровоизлияниями. В полостях тела — транссудат, количество к-рого достигает 30% веса тела плода (800 мл). Сердце, печень и селезенка значительно увеличены. Почки плотны и полнокровны, сохраняют выраженную эмбриональную дольчатость. Мягкая мозговая оболочка и ткань мозга отечны и полнокровны. Вил очковая железа атрофична. Имеются признаки недоношенности: задержка формирования ядер окостенения и др. При микроскопическом исследовании определяется значительный эритробластоз в печени (цветн. рис. 21), селезенке, лимф, узлах, почках. В костном мозге — преобладание ядросодержащих клеток эритроцитарного ряда. Отмечается умеренный гемосидероз органов. В сердце находят гиперплазию мышечных волокон. В печени, надпочечниках, головном мозге отмечаются кровоизлияния, дистрофические и некробиотические изменения, плазматическое пропитывание и фибриноидные изменения мелких сосудов. Изменения головного мозга характерны для состояния хронической гипоксии. Даже у доношенных плодов имеются признаки тканевой незрелости. Плацента отечна, с признаками преждевременной инволюции.
При анемической форме Г. б. н. выражены общая бледность покровов и малокровие внутренних органов. В печени и селезенке находят умеренный эритробластоз. Дистрофические и некробиотические изменения в органах незначительные. Изменения головного мозга выражены менее резко, чем при отечной форме. Смерть может наступить в период новорожденности от интеркуррентного заболевания.
Жeлтушная форма Г. б. н. характеризуется желтушностью покровов. В желтый цвет прокра-щены также подкожный жировой слой и интима крупных сосудов. Количество непрямого билирубина в сыворотке крови может достигать 20—40 мг% . В брюшной и плевральной полостях, в полости перикарда— небольшое количество прозрачной жидкости желтого цвета. Ядра головного мозга — гиппокамп, область дна ромбовидной ямки, нижние оливы, ядро подбугорья, бледное ядро, зубчатое ядро мозжечка — интенсивно прокрашиваются билирубином в охряно-желтый цвет (так наз. ядерная желтуха). Печень и селезенка увеличены. Последняя плотная, коричнево-красная на разрезе. В почках развиваются билирубиновые инфаркты (см.). В миокарде выявляются дистрофия и вакуолизация мышечных волокон. При микроскопическом исследовании обнаруживают дистрофические и некротические изменения (острое набухание, ишемические изменения) ганглиозных клеток головного мозга (цветн. рис. 23). Тяжесть поражения мозга усугубляется гипоксией из-за повреждений мелких сосудов. В печени и селезенке резко выражен гемосидероз (цветн. рис. 22), но эритробластоз менее значительный, чем при отечной форме. В печени, кроме того, обнаруживают желчные стазы, тромбы, иногда с образованием желчных камней.
Патофизиология
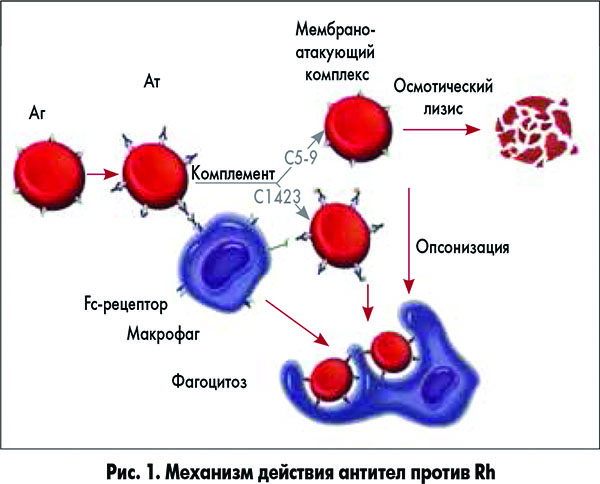
Антитела вырабатываются, когда организм подвергается воздействию антигена, чужеродного для организма. Если мать подвергается воздействию чужеродного антигена и продуцирует IgG (в отличие от IgM, который не проникает через плаценту), IgG будет нацеливаться на антиген, если он присутствует у плода, и может повлиять на него внутриутробно и сохраниться после родов. Три наиболее распространенных модели, в которых женщина становится сенсибилизированной к определенному антигену (т. Е. Вырабатывает антитела IgG против), — это кровотечение, переливание крови и несовместимость по системе АВО.
Кровоизлияние у плода и матери , которое представляет собой движение клеток крови плода через плаценту, может происходить во время аборта , внематочной беременности , родов , разрывов плаценты во время беременности (часто вызванных травмой) или медицинских процедур, проводимых во время беременности, которые нарушают стенка матки. При последующих беременностях, если у плода наблюдается аналогичная несовместимость, эти антитела могут проникать через плаценту в кровоток плода, прикрепляться к эритроцитам и вызывать их разрушение ( гемолиз ). Это основная причина ГБН, потому что 75% беременностей приводят к контакту между кровью плода и матери, а у 15–50% беременностей наблюдаются кровотечения с потенциалом иммунной сенсибилизации. Количество крови плода, необходимое для сенсибилизации матери, зависит от иммунной системы человека и колеблется от 0,1 мл до 30 мл.
Возможно, женщине сделали терапевтическое переливание крови . Типирование системы групп крови ABO и антигена D резус (Rh) системы групп крови является обычным делом перед переливанием. Были высказаны предложения, что женщинам детородного возраста или молодым девушкам не следует делать переливание Rhc-положительной крови или Kell 1 -положительной крови, чтобы избежать возможной сенсибилизации, но это приведет к перегрузке ресурсов служб переливания крови, и это в настоящее время считается неэкономичным проводить скрининг на эти группы крови. HDFN также может быть вызвана антителами к множеству других антигенов системы группы крови , но Kell и Rh встречаются наиболее часто.
Третья модель сенсибилизации может возникать у женщин с группой крови O. Иммунный ответ на антигены A и B, широко распространенные в окружающей среде, обычно приводит к продукции IgM или IgG анти-A и анти-B антител в раннем возрасте. Женщины с группой крови O более склонны, чем женщины с типом A и B, к выработке IgG-антител к A и анти-B, и эти IgG-антитела способны проникать через плаценту. По неизвестным причинам частота материнских антител против антигенов типа A и B типа IgG, которые потенциально могут вызвать гемолитическую болезнь новорожденного, выше, чем наблюдаемая частота «болезни АВО». Около 15% беременностей происходит от матери типа O и ребенка типа A или типа B; только 3% этих беременностей заканчиваются гемолитической болезнью из-за несовместимости A / B / O. В отличие от антител к антигенам A и B, резус-антитела обычно не образуются при воздействии антигенов окружающей среды. В случаях несовместимости по системе ABO и несовместимости по резус-фактору риск аллоиммунизации снижается, поскольку эритроциты плода удаляются из материнского кровотока из-за антител против ABO до того, как они могут вызвать анти-резус-ответ.
Специфические антитела
- Anti-D — единственная предотвратимая форма ГБН. После введения в 1968 г. иммуноглобулина Rho-D ( Rhogam ), который предотвращает выработку материнских антител Rho-D, заболеваемость анти-D HDN резко снизилась.
- И анти-C, и анти-c могут показывать отрицательный DAT, но все же имеют тяжелое поражение младенца. Непрямой Кумбс также должен быть запущен.
- Anti-M также рекомендует тестирование на антигены, чтобы исключить наличие HDN, поскольку прямые половые клетки могут дать отрицательный результат у серьезно пораженного ребенка.
- Anti-Kell может вызвать тяжелую анемию независимо от титра. Anti-Kell подавляет костный мозг, подавляя клетки-предшественники эритроидных клеток.
- Антигены Kidd также присутствуют на эндотелиальных клетках почек.
- Одно исследование, проведенное Мораном и др., Показало, что титры анти-E ненадежны. Их наиболее тяжелый случай гемолитической болезни новорожденных произошел с титрами 1: 2. Моран заявляет, что было бы неразумно отвергать анти-Е как имеющий незначительные клинические последствия.
Лечение ГБН

Начать лечение данного заболевания можно уже во время беременности, чтобы не допустить ухудшение состояние плода:
- Введение в организм матери энтеросорбентов, например “Полисорб”. Данный препараты способствует уменьшению титра антител.
- Капельное введение растворов глюкозы и витамина Е. Эти вещества укрепляют клеточные мембраны эритроцитов.
- Инъекции кровоостанавливающих препаратов: “Дицинон” (“Этамзилат”). Они нужны для повышения свертывающей способности крови.
- В тяжелых случаях может потребоваться внутриутробное переливание крови плоду. Однако, эта процедура очень опасна и чревата неблагоприятными последствиями: гибель плода, преждевременные роды и др.
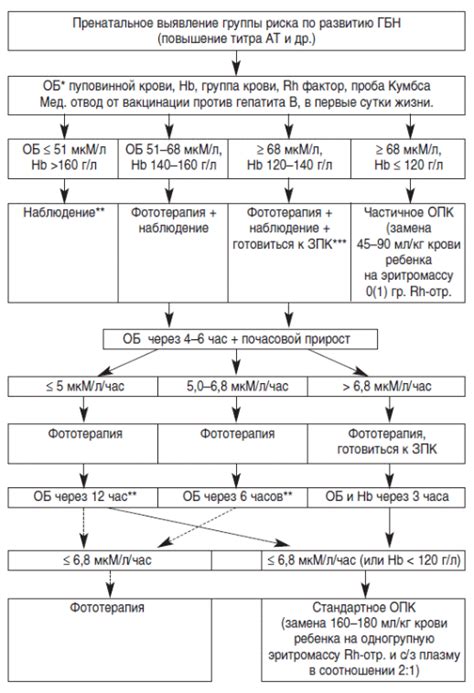
Методы лечения ребенка после родов:
Фототерапия. Благодаря воздействию света с определенной длиной волны (около 460 нм) в организме ребенка происходит превращение билирубина в его метаболит, который уже не является опасным и токсичным, а также хорошо выводится почками
Важно знать, что расстояние от источника света до тела малыша должно быть 50 см, и проводить лечение нужно длительным курсом, общая продолжительность которого должна составлять 70 часов. Необходимо делать 12-часовые перерывы между процедурами фототерапии.
Введение препаратов, препятствующих развитию геморрагических осложнений (“Дицинон”).
Необходимо улучшить работу печени (“Эссенциале”).
Проводить лечение, которое бы устраняло токсическое воздействие билирубина (“5% Раствор глюкозы”, “Аскорбиновая кислота”, “Токоферол”).
Применение энтеросорбентов.
Эффективно проведение очистительной клизмы в первые дни малыша, так как в первом стуле (меконии) присутствует большое количество токсических веществ.
При тяжелой степени заболевания применяют следующие методы лечения:
Переливание крови
Важно помнить, что для гемотрансфузии используется только “свежая” кровь, дата заготовки которой не превышает трех суток. Эта процедура опасна, но она может спасти жизнь малышу.
Очищение крови с помощью аппаратов гемодиализа и плазмафереза
Данные методы способствуют выведению из крови токсических веществ (билирубина, антител, продуктов разрушения эритроцитов).
Диагноз
Предположение о возможности развития Гемолитической болезни новорождённых должно возникнуть при обследовании беременной в женской консультации. Резус-отрицательная кровь у матери и резус-положительная у отца, указания в анамнезе матери на переливание крови без учета резус-фактора должны вызвать предположение о возможности Г. б. н. у ожидаемого ребенка. Наличие отягощенного акушерского анамнеза (мертворождения, самопроизвольные выкидыши, рождение детей с Г. б. н., отставание в психическом развитии старших детей) заставляет подумать о возможности более тяжелого течения Г. б. н. у ожидаемого ребенка, т. к. последующие беременности ведут к усилению сенсибилизации у изоиммунизированных женщин.
В таких случаях можно до рождения ребенка исследовать на антитела околоплодные воды, полученные с помощью амниоцентеза (см.). Наличие неполных антител в околоплодных водах говорит о конфликте средней тяжести или тяжелом, но отрицательный результат анализа не исключает возможности развития Г. б. н.
Ранний диагноз Г. б. н. и оценка тяжести заболевания должны быть проведены сразу после рождения ребенка. Наличие резус-отрицательной крови у матери и резус-положительной крови у новорожденного (при групповой несовместимости — наличие 0(I) группы у матери и А(II) или B(III) — у ребенка) и наличие резус-антител в сыворотке крови матери указывают на возможность развития Г. б. н. Для выяснения тяжести заболевания необходимо определить титр резус-антител (при высоком титре — начиная с 1 : 16 и выше — чаще имеют место тяжелые формы заболевания ребенка). При групповой несовместимости следует учитывать наличие высокого титра иммунных а- и (3-агглютининов (см. Группы крови). Как правило, в случае тяжелого течения диагноз не вызывает затруднений даже при отсутствии анамнестических данных: околоплодные воды и родовая смазка окрашены в желтый или зеленый цвет, ребенок отечный, желтушный или бледный, увеличены печень и селезенка. В неясных случаях имеет значение клин, анализ крови новорожденного, особенно пуповинной, т. к. изменения со стороны крови при Г. б. н. выявляются значительно раньше, чем другие клин, признаки заболевания. Диагностическое значение имеет снижение гемоглобина ниже 16,6 г%, наличие в крови нормобластов и эритробластов (больше чем 10 на 100 лейкоцитов), содержание билирубина в пуповинной крови выше 3 мг% по Ван-ден-Бергу, положительная проба Кумбса (см. Кумбса реакция) при резус-конфликте (при конфликте по системе AB0 — проба Кумбса отрицательная).
Рис. 2. Таблица Полачека для определения показаний к обменному переливанию крови в соответствии с динамикой билирубина у детей в первые дни жизни при гемолитической болезни новорожденных. При содержании билирубина выше верхней кривой показано обменное переливание крови, нише нижней кривой — обменное переливание крови не показано. При содержании билирубина, соответствующем промежутку между верхней и нижней кривыми, обменное переливание крови производится в зависимости от клинических данных.
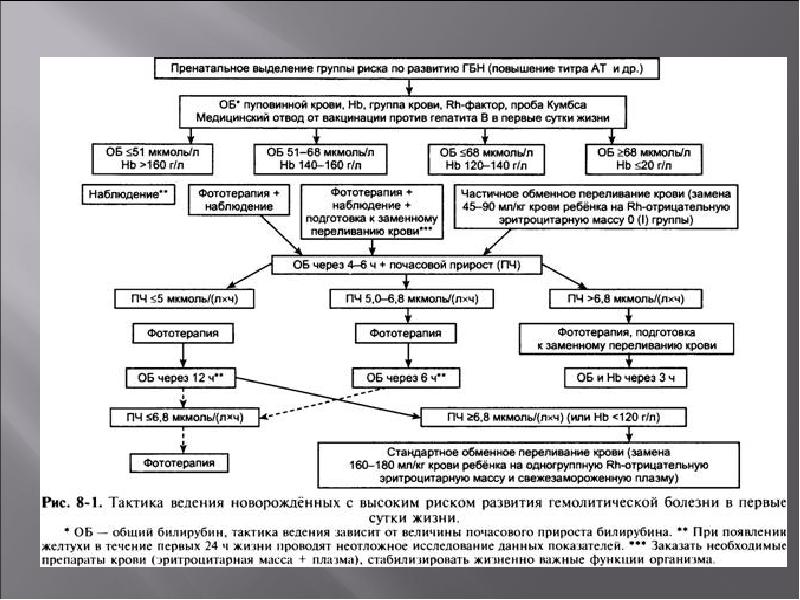
Трудно бывает поставить диагноз, если Г. б. н. вызвана другими антигенами. В таких случаях проводят исследования сыворотки крови на наличие антител и определение их титра. Ранняя диагностика Г. б. н. имеет значение для срочного проведения заменного переливания крови. Если же сразу при рождении сложно решить вопрос о тяжести Г. б. н., то можно провести оценку по таблице Полачека (К. Polacek) (рис. 2) или вычислить почасовой прирост билирубина по формуле В. А. Таболина:
Bt = (Bn2 — Bn1) / (n2-n1) мг%,
где: Bt — почасовой прирост билирубина; Bn1 — уровень билирубина при первом определении; Bn2 — уровень билирубина при втором определении; n1 — возраст ребенка в часах при первом определении билирубина; n2 — возраст ребенка в часах при втором определении билирубина.
Дифференциальный диагноз: надо исключить затянувшуюся физиологическую желтуху новорожденных (см. Желтуха, у детей), транзиторную негемолитическую гипербилирубинемию (см.), наследственные гемолитические анемии — сфероцитарную Минковского — Шоффара и несфероцитарную (см. Гемолитическая анемия, Энзимопеническая анемия), желтухи вследствие дефицита глюкуронилтрансферазы или семейную негемолитическую гипербилирубинемию с ядерной желтухой — так наз. синдром Криглера — Найярра (см. Гепатозы), желтуху и анемию при сепсисе (см.), цитомегалии (см.), токсоплазмозе (см.), врожденном сифилисе (см.) и других инфекционных заболеваниях, анемии при кровотечениях и кровоизлияниях и др.
В каких формах развивается ГНБ
ГБН у новорожденных имеет 3 формы.
 Желтуха у новорожденного
Желтуха у новорожденного
Самая распространенная форма ГБН
К ней относится гемолитическая желтуха у новорожденных по группе крови и резус-фактору. Она регистрируется в 88% появления ГНБ. Гемолитическая болезнь при резус-конфликте в желтушной форме проявляется непосредственно после рождения, при конфликте по системе АВО – на второй-третий день.
Симптомы
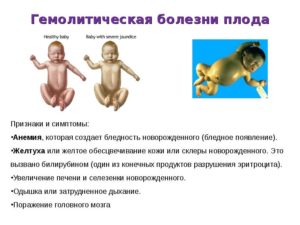
- Наиболее характерный признак – кожа и склеры младенца желтеют.
- Размеры печени и селезенки увеличиваются.
- Анализы показывают уменьшение концентрации гемоглобина и повышение билирубина, который и дает желтизну.
- Интоксикация билирубином приводит к изменениям в поведении малыша. Он становится вялым, у него падает мышечный тонус, наблюдается длительная зевота, судорожный синдром.
К концу первой недели появляются первые симптомы застоя желчи:
- бесцветный кал;
- темная моча;
- зеленоватый оттенок кожных покровов;
- повышение в крови конъюгированного или прямого билирубина (непрямой билирубин, переработанный печенью).
Чем опасна желтуха новорожденных
Нарастание концентрации непрямого билирубина представляет реальную угрозу для здоровья и жизни новорожденного, поскольку этот вид билирубина токсичен. При достижении определенного критичного уровня билирубин преодолевает гематоэнцефалический барьер между кровью и нервной тканью. Этот барьер защищает мозг от проникновения в него всего того, что там не должно быть, в том числе клеток иммунной системы. Для доношенного ребенка критичным является содержание непрямого билирубина – 340 мкмоль/л. Для недоношенного ребенка достаточно 200 мкмоль/л.
Попадая в мозг, непрямой билирубин повреждает подкорковые ядра. Развивается ядерная желтуха – самое опасное осложнение при желтушном течении ГБН. Младенец может не выжить или приобрести тяжелые последствия для здоровья (церебральный паралич, глухота).
Чтобы несколько успокоить родителей, стоит сказать, ядерная желтуха развивается не всегда при превышении уровня в 340 мкмоль/л.
- При данной концентрации она начинается только у каждого десятого больного ребенка.
- При концентрации 430 мкмоль/л заболевает каждый третий.
- Содержание сверх 520 мкмоль/ приводит к ядерной желтухе в 70% случаев.
Однако зарегистрированы эпизоды, когда она не развивалась и при 650 мкмоль/л. Научного объяснения этот факт пока не имеет.
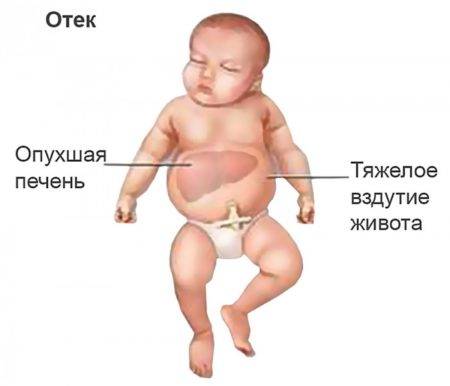 Отечная форма ГБН
Отечная форма ГБН
Самая редкая форма ГБН
Реже всего встречается отечная ее форма (около 2%). Она имеет самые тяжелые последствия. Другое название – внутриутробная водянка. Гемолитическая болезнь этой формы начинается во время беременности. Плод может погибнуть в утробе, родиться мертвым. При рождении живым ребенок редко проживает более двух дней.
Симптомы
- Наблюдается значительная отечность подкожной клетчатки.
- Излишнее количество жидкости содержится в плевральной, брюшной и других полостях.
- Цвет кожи очень бледный, иногда с желтоватым оттенком.
- Размеры селезенки и печени сильно увеличены.
- У ребенка характерное лунообразное лицо.
- При анализе крови обнаруживается малое количество эритроцитов и гемоглобина, излишек лейкоцитов и незрелых эритроцитов.
Самая легкая форма ГБН
Таковой является анемичная форма (10%). Впрочем, эта легкость имеет относительный характер. Она легкая по отношению к двум другим формам ГБН. Иногда может развиться в тяжелую анемию.
Симптомы
- Кожа новорожденного имеет бледный цвет, но не всегда.
- Селезенка и печень увеличены, но меньше, чем при двух предыдущих формах.
- Общее состояние ребенка неплохое, только опытный врач может заподозрить неладное.
- В анализе крови фиксируется небольшое превышение нормы непрямого билирубина.
Тяжелая анемия может развиться через две-три недели при отсутствии лечения.
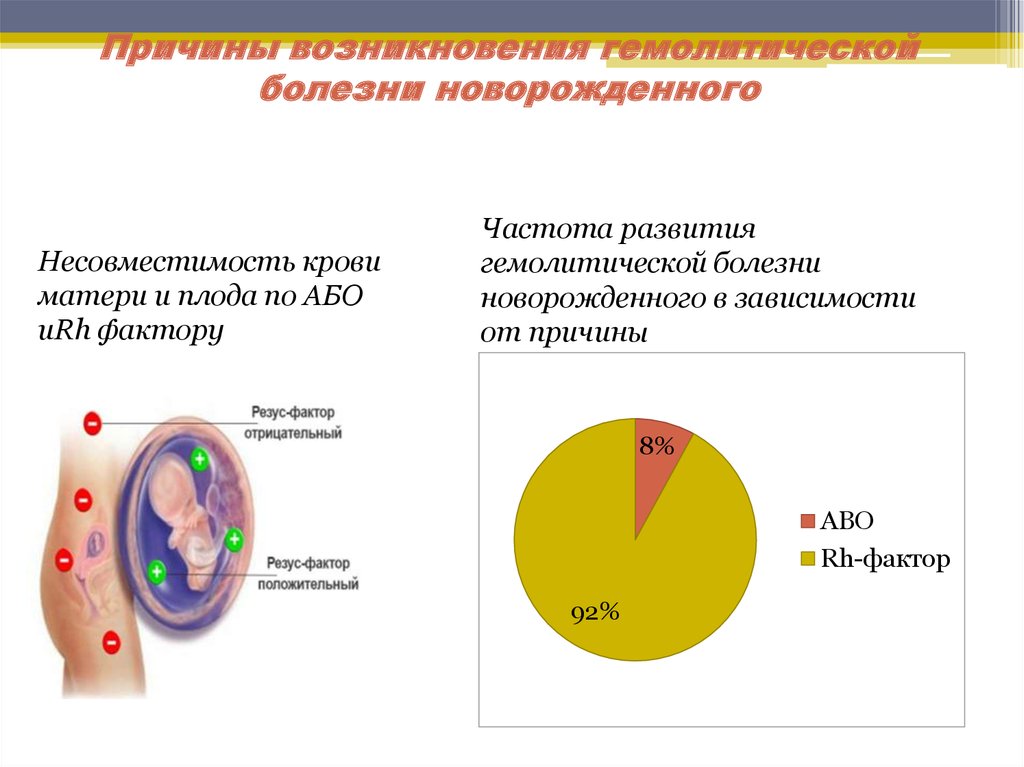
Прогноз по группе крови и резус-фактору
 Чаще наблюдается несовместимость по резус-фактору, реже — по групповым антигенам
Чаще наблюдается несовместимость по резус-фактору, реже — по групповым антигенам
Для полноты понимания сущности процессов стоит вспомнить значение понятий «резус-конфликт» и «несовместимость плода и матери», а ещё разобраться в причинах вероятной несовместимости иммунитетов беременной женщины и плода.
Резус-фактор и возникновение конфликта по этому признаку
Резус-фактором именуют особый белок, которые находится на поверхности красных частиц крови. Такой элемент присутствует не у каждого человека, поэтому:
- имеющие его считаются носителями резус-положительного фактора крови (таких 85%);
- те, кто не имеет, относятся к категории резус-отрицательных (их не более 15%).
Чтобы определить, есть ли этот белок в красных элементах крови конкретного человека, проводится специальный генетический тест. Он, как и анализ на групповую принадлежность, входит в число обязательных при беременности и выполняется для определения вероятности конфликта, а также для его профилактики.
Несовместимость по признаку резуса формируется как ответ иммунной системы будущей матери на соответствующую характеристику эритроцитов малыша. Когда женский организм классифицирует резус-белок плода как чужеродный, иммунитет пытается его уничтожить путём выработки специфических антител. Попадая в кровяное русло плода, эти элементы разрушают эритроциты. Одновременно происходит высвобождение токсического билирубина, который пагубно влияет на органы и ткани маленького организма, представляя особую опасность для ЦНС. Чтобы переработать уничтоженные клетки, селезёнка и печень начинают функционировать в режиме повышенной нагрузки и увеличиваются в объёме. Происходят и другие патологические изменения. В комплексе это запускает механизм развития гемолитической болезни.
Материнские антитела, попавшие в кровоток малыша во внутриутробный период, остаются там и после его появления на свет. Таким образом гемолитическая болезнь плода трансформируется в одноимённую патологию новорождённого, опасную своими последствиями.
Антитела к плоду не исчезают из организма женщины после родоразрешения. Они остаются на всю жизнь и несут риск резус-несовместимости для каждой новой беременности. Примечательно, что опасность конфликта при самом первом вынашивании существенно ниже, чем при последующих.
Конфликт по признаку группы крови и его проявления
Эритроциты крови первой группы свободны от антигенов А и В, но имеют антитела альфа и бета. Во всех других группах такие антигены имеются, поэтому первая, столкнувшись с непонятными для себя элементами А или В, определяет их как чуждые и начинает активную «войну». Происходит уничтожение красных элементов крови, содержащих эти антигены.
Теоретически предпосылкой к такому развитию событий могут стать определённые сочетания групповой принадлежности крови беременной и плода.
Таблица: потенциально опасные сочетания групп крови матери и плода
| Группа крови | |
| Женщины | Плода |
| I или III | II |
| I или II | III |
| I, II или III | IV |
Наиболее опасным, с точки зрения перспективы гемолитических отклонений, считается положение, когда у беременной I группа крови, а у будущего новорождённого II или III.
В список риска также входят женщины, которые:
- пережили хотя бы однажды переливание крови или эритроцитарной массы;
- имеют в анамнезе невынашивание беременности или медицинский аборт;
- воспитывают кровного ребёнка, отстающего от сверстников в умственном и психическим развитии в связи с перенесённой гемолитической патологией.
Кроме того, риск иммунного конфликта беременной и плода имеется, когда кровь будущих отца и матери сочетается следующим образом.
Таблица: потенциально опасные сочетания групп крови матери и отца
| Женщина | Мужчина |
| I | II, III или IV |
| II | III или IV |
| III | II или IV |
Семьям, которые планируют детей, но переживают по поводу вероятной несовместимости крови, важно знать, что:
- риск его развития именно по этому признаку крайне мал;
- даже если несовместимость проявилась, она протекает относительно легко, если сравнивать ситуацию с резус-конфликтом.
В медицинской практике бывают тяжёлые, осложнённые случаи, но нечасто.
Лечение
В условиях стационара терапию проводят врачи – неонатолог, гематолог и педиатр. Используется комплекс лечебных мероприятий, зависящий от формы и тяжести болезни.
Неинвазивные методы
Лечение беременной на последних неделях включает плазмаферез и стимуляцию иммунной защиты иммуноглобулинами. Это способствует уменьшению интоксикации организма, снижению содержания антител в крови и последующего транспорта через плаценту плоду.

Введение иммуноглобулинов на протяжении последних 3-х недель курсом не оказывает существенного влияния на состояние крови плода, метод применяют выборочно, он не общепризнан.
Инвазивные методы
Используются следующие способы лечения ГБН, относящиеся к инвазивным:
- до родов для плода – кордоцентез, трансфузия «отмытых» эритроцитов крови;
- для новорожденного – устранение гипербилирубинемии, анемии, симптоматическая терапия, исходя из особенностей развития болезни.
Симптоматическая терапия при болезни крови предполагает вливания свежезамороженной плазмы, тромбоцитарной массы, препаратов, усиливающих диурез. После переливаний крови и улучшения состояния формируется поддерживающая терапия, проводятся контрольные анализы крови.
Фототерапия
Для разрушения непрямого билирубина в кожном слое используют фототерапию. Действие флуоресцентных ламп основано на окислении НБ, превращении его в нетоксичные соединения и последующем выводе из организма.
Продолжительность проведения фототерапевтического лечения устанавливают по стойкому снижению НБ в крови.
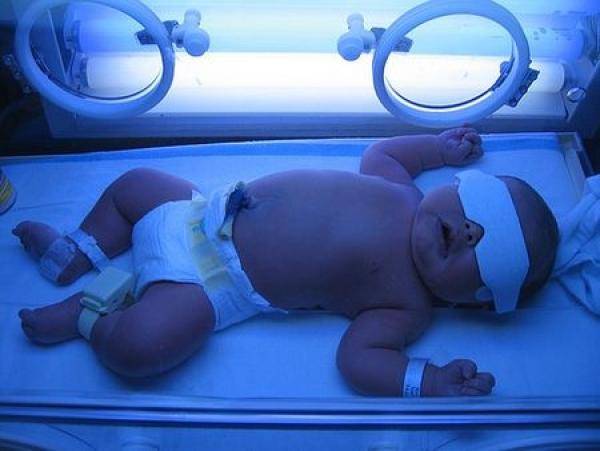
Применение иммуноглобулина
Введенный плоду иммуноглобулин (быстро, через 1-2 часа после рождения) помогает предотвратить массовый гемолиз эритроцитов. Препарат снижает необходимость частых заменных переливаний крови и продолжительной фототерапии, так как они имеют побочные эффекты.
Инфузионная терапия
Введение лекарственных растворов проводится вместе с фотолечением и усиливает его действие. Задача инфузионной терапии – ускорение диуреза, увеличение ввода жидкости для вымывания опасных веществ из организма новорожденного. Обычно вводится 10 % раствор глюкозы. К нему добавляют при необходимости другие препараты – Но-шпу, растворы калия хлорида, сульфата магния. Вещества при гемолитической болезни вводятся внутривенно или через желудочный зонд.
Оперативная терапия
Заменное переливание крови (ЗПК) младенцу относят к способам оперативной терапии ГБН. Выполняют маятниковым способом – удаляется часть крови, затем вливается. Проводится при гемолитической болезни в следующие сроки:
- раннее ЗПК – в течение первых двух суток жизни;
- позднее – начиная с 3-х суток.

Показаниями к проведению переливания при ГБН являются:
- быстрый рост непрямого билирубина (6 микромоль на литр в час);
- признаки билирубиновой интоксикации;
- крайне тяжелое состояние – отечность органов, анемия, желтуха в первые часы жизни;
- тяжелые формы анемии.
При появлении интоксикации ЗПК проводится немедленно.
Выбор препаратов для заменного переливания крови
Для ЗМК используют:
- (Rh-) кровь (хранение 2-3 дня) одной группы с ребенком – при резус-конфликтной ситуации;
- соединение эритроцитов 0(1) группы, сочетающихся с резус-фактором ребенка, и плазмы АВ(IV) группы или такой, как у малыша – при групповой несовместимости (система АВО);
- группа эритроцитов 0(1) группы (резус-фактор минус) и плазма АВ(IV) группы или такой, как у новорожденного – при несовместимости по системе АВО и резус-конфликте одновременно.
Если конфликт по редким факторам, кровь выбирают индивидуально, в соответствии с группой, резус-фактором. Ищут подходящего донора без наличия конфликтных признаков.
Симптомы и признаки
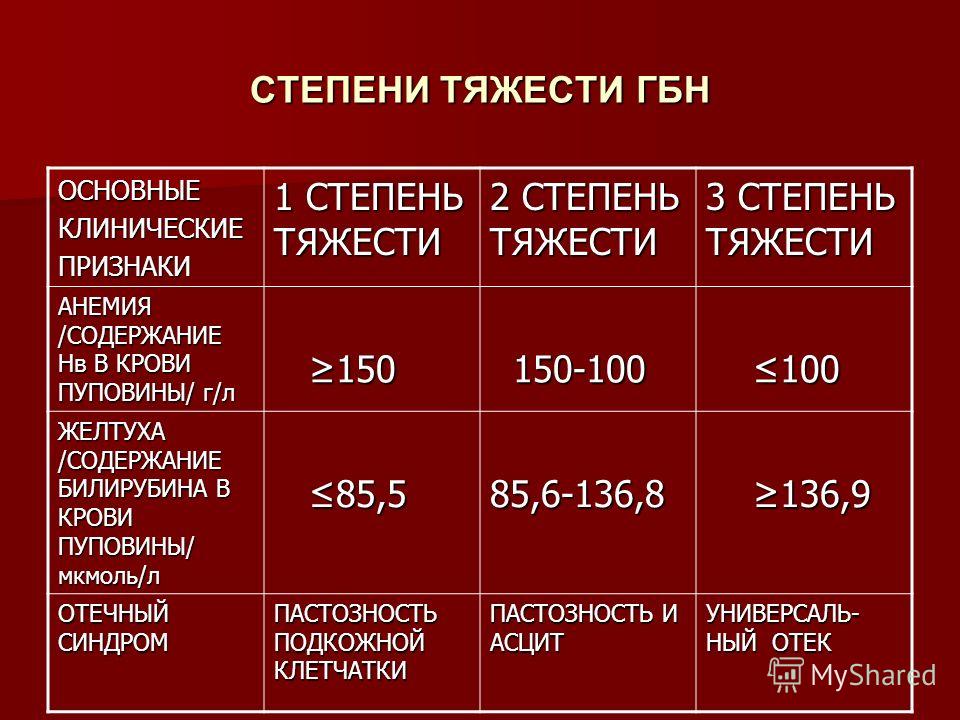
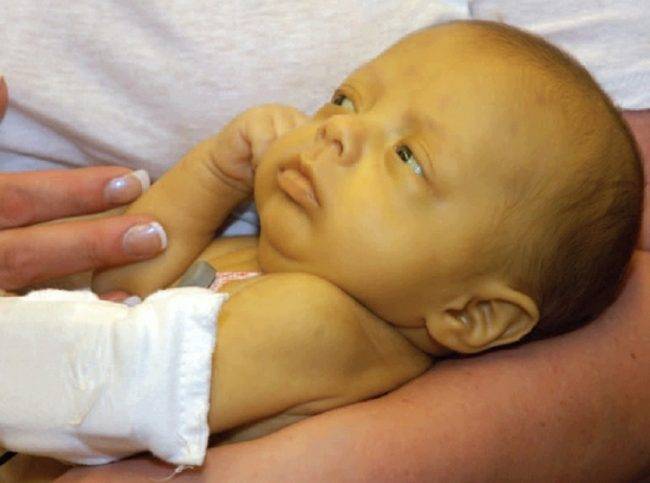 Гемолитическая болезнь новорождённых бывает разной по форме и степени тяжести — от лёгкой до крайне тяжёлой степени тяжести заболевания
Гемолитическая болезнь новорождённых бывает разной по форме и степени тяжести — от лёгкой до крайне тяжёлой степени тяжести заболевания
Характер проявлений гемолитической патологии новорождённых зависят от её формы.
Желтушная
При желтушной — самой распространённой — исследование крови показывает чрезмерный уровень желчного пигмента — билирубина. Если в норме он составляет от 10,2 до 51 мкмоль/л , то у больных детей гораздо выше, что объясняется процессом масштабного разрушения эритроцитов. В случае повышения билирубина до критических цифр не исключено развитие нарушений церебрального характера, так как желчный пигмент преодолевает гематоэнцефалический барьер и наносит вред ЦНС плода. Подобное состояние именуется ядерной желтухой и проявляется следующим образом:
- сначала возникает общая вялость, падает АД, снижаются рефлексы. Ребёнок часто зевает, срыгивает пищу частично или полностью. Ест неохотно, крик его становится монотонным.
- на 3–4 сутки происходят затяжные остановки дыхания, снижение частоты сердечного ритма. Ребёнок закатывает глаза, плохо реагирует на раздражители. Апатичное и малоподвижное состояние может резко сменяться двигательной активностью и судорогами;
- к концу первого месяца неврологические симптомы сглаживаются и дают картину якобы выздоровления;
- с возраста 3–5 месяцев неврологические отклонения снова становятся заметны.
Другими типичными признаками желтушной формы являются светло-жёлтый окрас слизистых и кожи, а также увеличенная селезёнка. Не исключено появление отёков из-за проблем с выработкой белка в печени, размер которой тоже больше нормы.
Ребёнок, как правило, появляется на свет в положенный срок, с массой тела в пределах допустимого и нормальным цветом кожи. Однако через 1–2 дня появляются признаки желтухи, которые нарастают вплоть до 4 суток, но затем уходят в результате лечения. В это период моча ребёнка становится тёмной, как пиво, а кал сохраняет нормальную окраску. Реже случается так, что малыш рождается уже с жёлтым оттенком тела. Околоплодная жидкость и первородная смазка имеют такой же цвет.
Анемическая
Анемическая форма характеризуется пониженным гемоглобином и гематокритом. В числе её проявлений:
- патологическая бледность тела новорождённого;
- незначительное увеличение печени, реже — селезёнки.
В некоторых случаях симптомы анемической формы заметны уже при появлении на свет, но чаще они появляются ко 2-й неделе жизни в результате стремительного развития патологии. Помимо низкого гемоглобина, анализы крови показывают дефицит молодых форм красных кровяных клеток, при этом показатель непрямого билирубина невысок.
Отёчная
Отёчная форма считается самой опасной потому, что в особо тяжёлых случаях становится причиной смерти ребёнка ещё до рождения или в первые часы/дни после появления на свет. Среди её проявлений:
- признаки анемии;
- свободная жидкость в брюшной полости (водянка);
- выпоты в лёгких (гидроторакс);
- увеличение печени и селезёнки, которые работают с повышенной нагрузкой, но едва справляются со своими функциями;
- нарушение сердечного ритма;
- бледность кожи с признаками кровоизлияний и мацерации (размягчения, в связи с нахождением в околоплодной жидкости).
Отсутствие желтушности при появлении на свет объясняется выведением неконъюгированного билирубина будущего ребёнка через структуры плаценты, а также его разбавлением в результате увеличения объёма циркулирующей крови и плазмы (гиперволемии).
Анализы крови выявляют:
- гипопротеинемию (количество сывороточного белка в крови меньше 40–45 г/л), высокую проницаемость сосудов;
- тяжёлую форму анемии (гемоглобин в пределах 35–50 г/л, число эритроцитов от 1,0 до 1,5 • 10–12/л). Как следствие, возникает дефицит кислорода в тканях;
- большое количество незрелых или аномальных форм эритроцитов (эритробластоз).
В большинстве случаев новорождённые с отёчной разновидностью имеют низкие баллы по АПГАР из-за выраженной сердечной, а также дыхательной недостаточности. Многие требуют реанимации сразу после появления на свет. Нередко положение осложняется появлением ДВС-синдрома и развитием шоковых состояний.
Новорождённые, не получившие должной терапии, в том числе частичной замены крови в первые часы жизни, умирают из-за нарастающей полиорганной недостаточности.
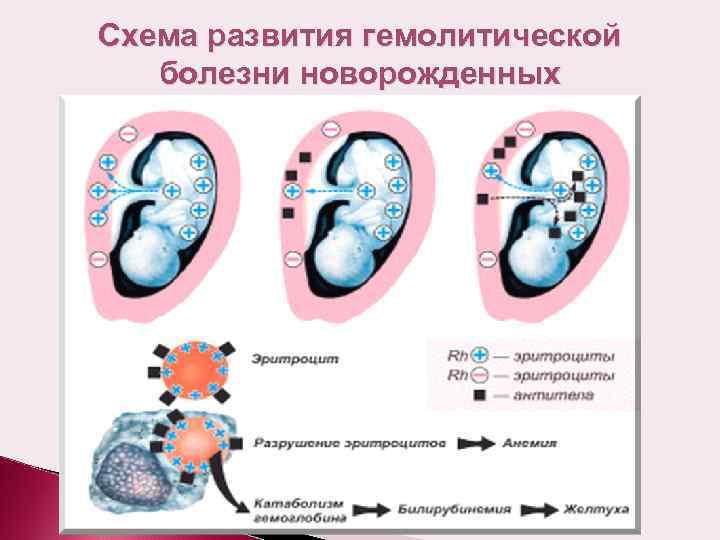
Причины и картина развития гемолитической болезни новорожденного и плода
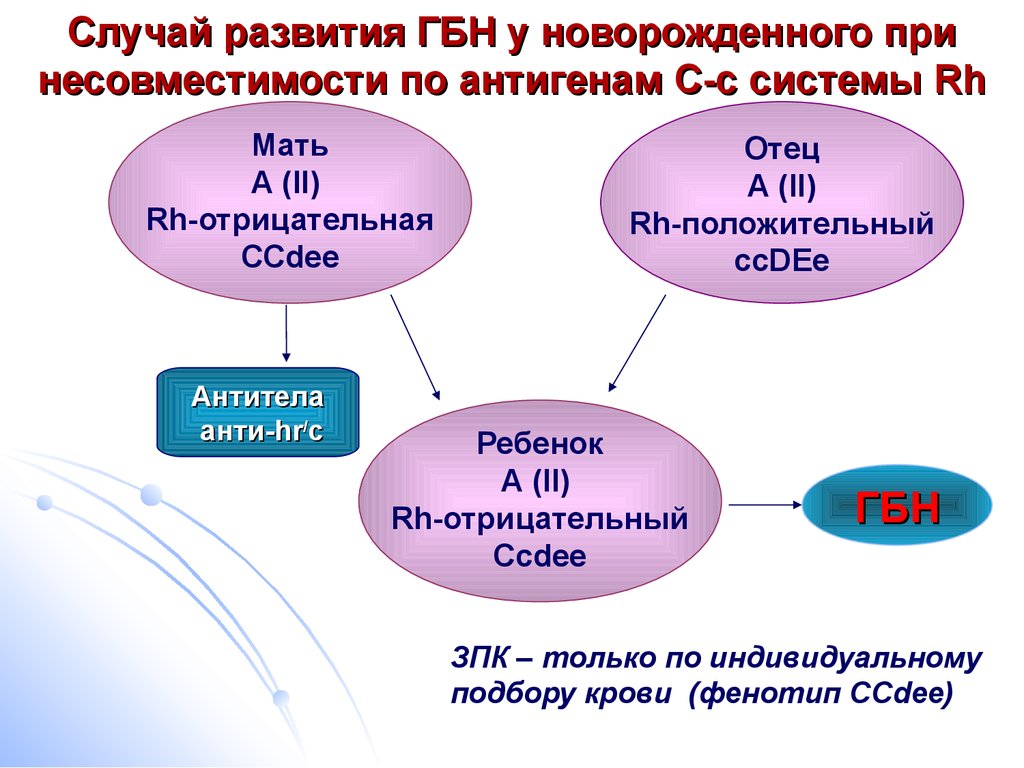
Причиной гемолитической болезни новорожденного является резус-несовместимость родителей ребенка. Заболевание диагностируют приблизительно у 0,5 % всех новорожденных. В России в 2013 г. ГБПиН была диагностирована у 0,83% новорожденных. Известны 14 основных эритроцитарных групповых систем, объединяющих более 100 антигенов, а также многочисленные частные и общие с другими тканями эритроцитарные антигены. Эритроциты ребенка всегда имеют какие-то отцовские антигены, отсутствующие у матери. Вместе с тем ГБПиН обычно вызывает несовместимость плода и матери по резус- или АВО-системе, редко по другим антигенным системам ввиду их меньшей иммуногенности (Kell, Duffu, Kidd, S, M, Lewis).
Учитывая причину гемолитической болезни плода, основным повреждающим фактором является осложнение повышенного гемолиза — гипербилирубинемия с неконъюгированным билирубином. Тяжесть поражения плода зависит от повреждающего действия антител, их титра и длительности воздействия, проницаемости плаценты, реактивности плода и его компенсаторных возможностей.
Картина развития гемолитической болезни новорожденных и плода выглядит следующим образом. Антигенная резус-система состоит из 6 основных антигенов (синтез которых определяют 3 пары генов), обозначаемых либо С, с; D, d, Е, е (терминология Фишера), либо RhI, hrl; Rho, hro; Rhll, hrll (терминология Виннера). «Резус-положительные эритроциты» содержат D-фактор, а так называемые резус-отрицательные эритроциты его не имеют, хотя в них обязательно есть (за редчайшим исключением) другие антигены резус-системы, в частности d. Несовместимость по антигенам АВО-системы, приводящая к гемолитической болезни новорожденного (ГБН), обычно развивается при группе крови матери 0(1) и группе крови плода А(П) или В(Ш). Крайне редко ГБПиН развивается, если у матери А(Н), а у плода — В(Ш) или AB(IV) группа крови, а также при В(Ш) группе крови у матери и А(П) или AB(IV) — у ребенка.
Обычно при резус-конфликте дети с ГБН рождаются от 2-3-й беременности, реже от 1 -й — при сенсибилизации в прошлом переливаниями крови без учета резус-фактора. При АВ 0-несовместимости заболевание развивается у ребенка уже от 1-й беременности. Тяжесть состояния ребенка и риск развития ядерной желтухи при ГБН по АВ0-системе менее выражены по сравнению с ГБНиП по резус-фактору. Это объясняется тем, что групповые антигены А и В экспрессируются многими клетками организма, а не только эритроцитами, что приводит к связыванию значительного количества антител в некроветворных тканях и препятствует их гемолитическому воздействию.
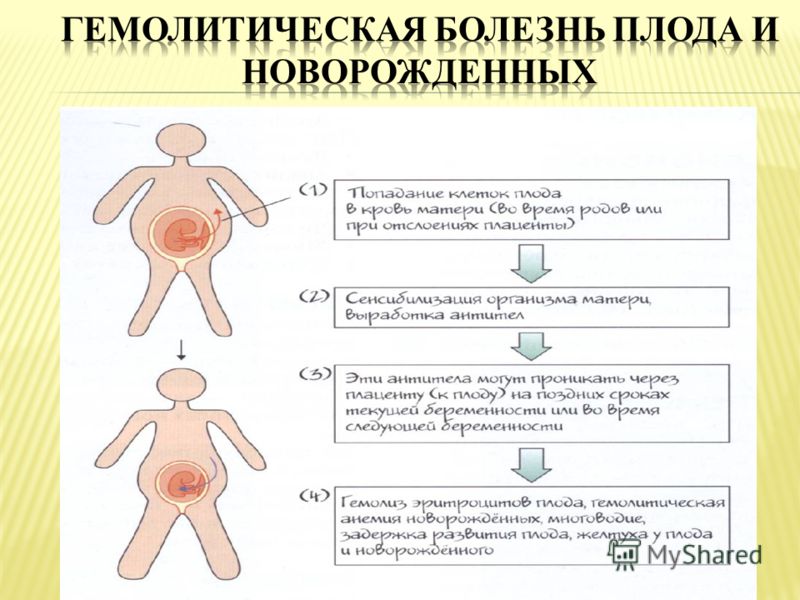
При несовместимости крови матери и плода в организме беременной вырабатываются антитела, которые проникают через плаценту в кровь плода и вызывают разрушение его эритроцитов. Нормальная плацента здоровой женщины непроницаема для антител. Она становится проницаемой лишь при различных заболеваниях и патологических состояниях беременности, а также во время родов. При проникновении антител в плод во время беременности развитие гемолитической болезни новорожденного происходит внутриутробно.